上面加少量氯酸钾,并在混合物中间插一根镁条,点燃镁条,观察发生的现象4可以看到镁条剧烈燃烧,放出一定的热量,使氧化铁粉沫和铝粉在较高的温度下发生剧烈的反应,放出大量的热,同时纸漏斗被烧穿,有熔融物落入沙中 反应物为铝粉难熔金属氧化物产物为难熔金属和三氧化二铝 高中;高中化学71个秒杀选择题技巧中部分知识点的总结如下元素与健康山区粗脖子病甲状腺肿大呆小病克汀病病因是缺碘,医生建议多吃海带进行食物疗法儿童常患软骨病是由于缺少钙元素金属及其用途制取包装香烟糖果金属箔的金属是铝比黄金熔点高约3倍,常用来制白炽灯泡灯丝的金属是钨用来制。
铝热剂通常由铝粉和三氧化二铁粉末按一定比例配成铝粉作为还原剂,三氧化二铁作为氧化剂引燃剂在铝热反应中,为了引发反应,通常需要加入引燃剂高中化学教材中多用镁条做引燃剂,氯酸钾做助燃剂镁条燃烧产生的热量足以点燃铝热剂,而氯酸钾则能加速燃烧过程三铝热反应的过程 当铝热剂被引燃;氢氧化镁MgOH?白色沉淀,不溶于水,溶于酸四铝及其化合物 铝的物理性质 银白色金属,有光泽,有良好的延展性和导电导热性密度较小,熔点较低,但沸点很高铝的化学性质 与氧气反应在常温下与氧气反应生成致密的氧化铝薄膜4Al + 3O? = 2Al?O?与酸反应与稀硫酸反应生成硫酸铝和氢气2。
高中化学原电池电极方程式核心知识点总结 原电池电极方程式的书写需遵循氧化还原反应规律和电解质环境特性,核心要点包括电极判断反应式配平及环境适配以下结合典型电池案例分类说明一金属空气电池以氧气为正极活性物质铝镍电池NaCl溶液,O?参与负极Al4Al 12e? = 4Al3?铝被。
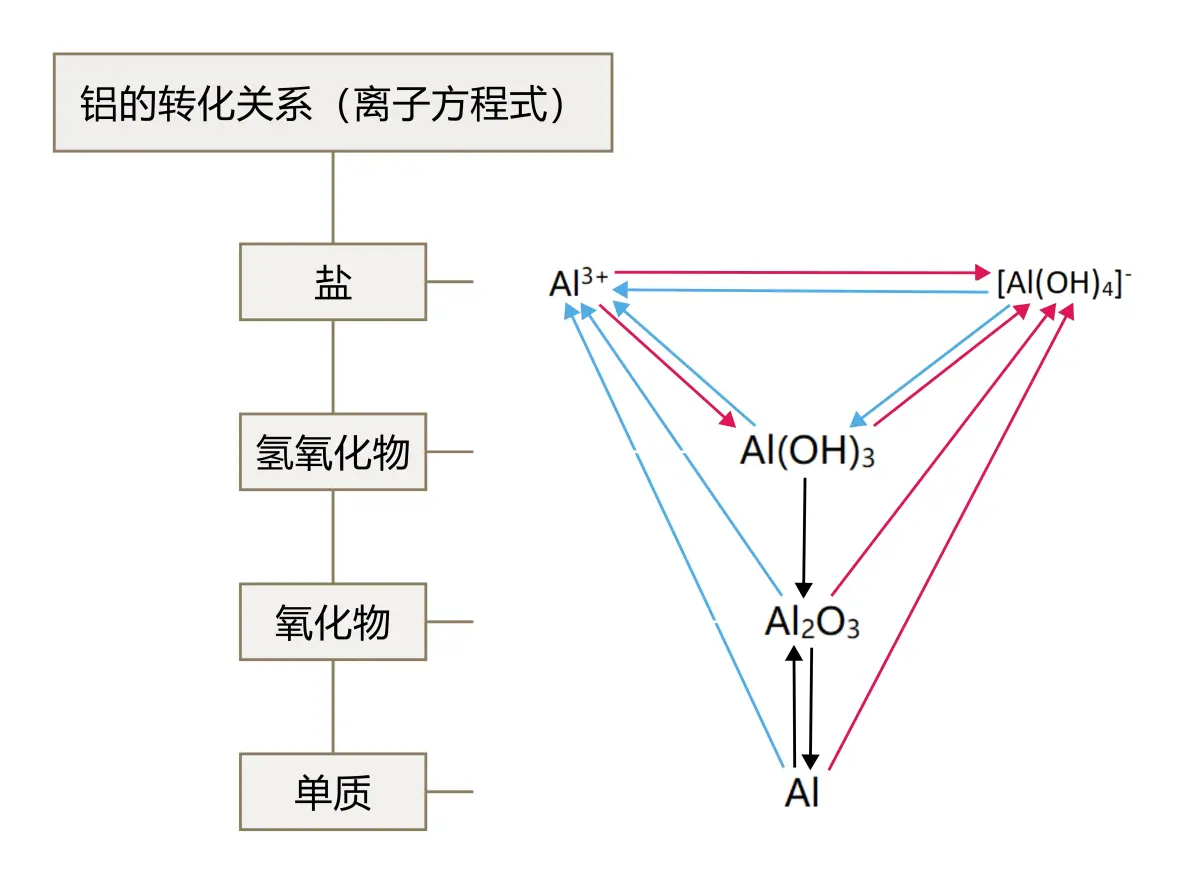
高中化学金属铝思维导图
点评铝及其化合物具有一些独特的性质,如铝与碱的反应Al2O3AlOH3分别是两性氧化物两性氢氧化物利用铝能与碱反应而其他金属不能,经常出现在实验题中,有关AlAl3+AlO2的离子共存问题,也是高考的热点 高中化学金属知识点铁及其化合物 1铁的化学性质 铁在金属活动性顺序表中排在氢的前面。
金属活动顺序的含义金属活动顺序,就是指金属的活跃程度,代表了金属的反应活性在金属活动顺序表中,金属的位置越靠前,其金属性越强,原子的还原性也越强反之,金属的位置越靠后,其金属性越弱,原子的还原性也越弱初高中化学中的金属活动性顺序钾钡钙钠镁铝锰等金属位于顺序。

是指染棉织品时的媒染剂铝后来的拉丁名称aluminium和元素符号Al正是由此而来1825年丹麦化学家奥斯德发表实验制取铝的经过1827年,德国化学家武勒重复了奥斯德的实验,并不断改进制取铝的方法1854年,德国化学家德维尔利用钠代替钾还原氯化铝,制得成锭的金属铝1。
并留给学生的思考问题这节课我们了解了金属和非金属之间的相互作用,那么非金属单质及化合物之间存在什么作用?为下节课的学习做好铺垫 5高中化学课件 教学重点 1影响盐类水解的因素,与水解平衡移动 2盐类水解的应用 教学难点盐类水解的应用 教学设计 师生共同巩固第一课时相关 1根据盐类水解规律分析 醋酸钾。
也进一步体现了铝热反应中氧化剂的重要性在铝热反应中,氧化剂不仅促进了反应的进行,还确保了反应的高效和稳定总的来说,铝热反应是一种在特定条件下发生的化学反应,其特点在于能放出大量的热和光,且常用于冶炼高熔点的金属在这个过程中,镁条和氯酸钾等物质的加入起到了至关重要的作用。
分析工艺流程对于化学工艺流程题,要认真分析工艺流程的原理和各步骤的作用可以通过绘制工艺流程图标注各物质的转化关系等方式,帮助自己理解工艺流程示例在从铝土矿中提炼铝的工艺流程中,可以绘制如下工艺流程图通过绘制工艺流程图,可以清晰地看到铝土矿经过一系列反应和操作后,最终得到金属铝的。
1 高中化学中,两性物质的定义是指它们能够与酸和碱都发生反应的物质例如,金属如锌Zn铝Al锡Sn铅Pb铍Be以及俗称为两性金属的铬Cr都能够形成两性氧化物或氢氧化物,如氧化锌ZnO和氢氧化锌ZnOH22 另一类两性物质是指那些能够接受和提供质子的分子,也就是。
22硅酸盐工业 新型无机非金属材料一硅酸盐工业1 水泥工业 原理石灰石与黏土在高温下发生复杂的物理化学变化,制得水泥熟料,再加入适量石膏并研成细粉就得到普通水泥主要原料石灰石和黏土设备水泥回转窑水泥的性质水泥加水搅拌后,能在水中硬化并在空气中继续硬化,最后变成坚硬的固体。
金属铝的化学性质ppt
1、高中化学中,金属相关的化学方程式是学习的重点以下是必须掌握的52个金属化学方程式,这些方程式涵盖了金属与酸碱盐的反应,以及金属的氧化还原反应等核心知识点一金属与酸的反应 锌和稀硫酸反应 Zn + H_2SO_4 = ZnSO_4 + H_2 uparrow 镁和稀硫酸反应 Mg + H_2SO_。
2、高中化学必修一二方程式汇总 高中化学必修一和必修二涉及众多重要的化学方程式,这些方程式是理解化学反应掌握化学原理的基础以下是对这两册教材中关键化学方程式的汇总一必修一化学方程式 金属及其化合物的性质 钠与氧气的反应常温4Na + O#8322 = 2Na#8322O 点燃2Na + O#8322。
3、高中化学学习需从基础记忆课堂重点做题总结方程式记忆特例积累及实验观察等方面入手,系统提升学习效果具体方法如下掌握化学基础元素与规律化学元素周期表金属活泼顺序氧化还原规律是高中化学的核心基础,需优先记忆可通过顺口溜如“钾钙钠镁铝,锌铁锡铅氢”组队互考等方式强化。
4、在高中化学学习中,铁铜铝等金属矿石是常见的研究对象铁矿石主要有磁铁矿Fe3O4四氧化三铁赤铁矿Fe2O3三氧化二铁菱铁矿FeCO3碳酸亚铁和黄铁矿FeS2二硫化亚铁这些矿石因其化学性质和物理特性,常用于提炼铁铜矿石则包括孔雀石Cu2OH2CO3碱式碳酸铜黄铜矿CuFeS。
5、金属在自然界中的存在形式主要有两种游离态和化合态化学性质不活泼的金属,如金Au银Ag铂Pt和铜Cu,能在游离态的形式下存在于自然界而化学性质较为活泼的金属,如铝Al和钠Na,则在自然界中以化合态的形式存在值得注意的是,虽然少数金属能以游离态形式出现,但大多数金。


发表评论